COPD oplossing dichterbij door ontwikkeling minilong
Overzicht
Mini-organen in opkomst
Dankzij revolutionaire ontwikkelingen in het stamcelonderzoek kunnen wetenschappers in het lab mini-organen kweken.
Een state-of-the-art techniek die medische doorbraken in regeneratief onderzoek kunnen versnellen.
Na de darm en alvleesklier, lukt dat sinds kort met nieren.
Om ook de complexe minilongen te realiseren, is internationale samenwerking vereist. In LONGFONDS | Accelerate werken toponderzoekers wereldwijd samen om met deze techniek een oplossing te vinden voor nu nog ongeneeslijke longziekten.
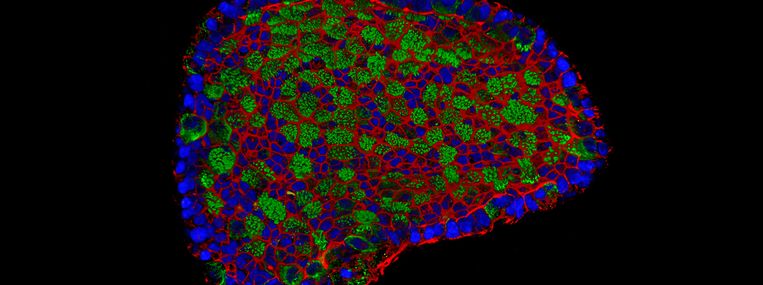
Organoïd van een stukje longBeeld Hubrecht Instituut
Door Naomi van Esschoten
Tien jaar geleden, kweekte prof.dr. Hans Clevers als eerste wetenschapper een minidarm, gevolgd door een minimaag en minilever.
En afgelopen maand is zijn onderzoeksgroep aan het Hubrecht Instituut geslaagd in het maken van mininieren en eierstokken. ‘Organoïden, zoals deze mini-organen worden genoemd, zijn een prachtig onderzoeksplatform om nieuwe medicijnen te testen.’ zegt Clevers.
‘Voor de complexe longen is het maken van een organoïde nog maar deels gelukt.
Ik verwacht dat we de komende tijd grote stappen kunnen maken, omdat we dankzij het Longfonds nu met experts van over de hele wereld samenwerken.’
Stamcel uit de pas
De mini-organen worden gekweekt uit stamcellen.
Deze moedercellen in organen produceren hun leven lang nieuwe dochtercellen, in de juiste hoeveelheid.
Maar als de stamcel verstoord raakt, gaat het mis. Clevers:
‘Bij COPD gaan longblaasjes kapot en worden niet meer gerepareerd of vervangen.
Wellicht komt dit omdat de stamcel uitgeput is geraakt van het continu beschadigingen repareren.
Maar het is ook mogelijk dat de stamcellen niet meer voldoende groeifactoren bevatten om de productie op peil te houden.’
Prof.dr. Hans Clevers, Consortiumleider Longregeneratie en professor Moleculaire Genetica aan de Universiteit UtrechtBeeld Longfonds
Bewegende trilharen
Clevers gebruikt de stamcellen om er in het lab mini-organen mee te kweken.
Clevers: ‘We zijn er al in geslaagd om uit stamcellen een miniluchtpijp te kweken.
Maar de longblaasjes zijn lastiger.
De uitdaging ligt enerzijds in de complexiteit van de structuur van longblaasjes, en anderzijds in de spilfunctie die ze vervullen: longblaasjes zorgen dat het bloed zuurstof opneemt.
Als we erin slagen de longblaasjes te kweken, kunnen we dus de belangrijkste eigenschappen van een menselijke long nabootsen in het lab.’
Opkikkerende cocktail
Zodra de organoïde van de long er is, verwacht Clevers precies te achterhalen waarom longblaasjes bij COPD zich niet meer herstellen. ‘Vervolgens kunnen we gericht behandelmogelijkheden ontwikkelen.
De huidige medicatie gaan de voortschrijdende beschadigingen niet tegen.
Wij willen kijken naar manieren waarop dat straks wel mogelijk is.
Als de stamcel uitgeput is, is het transplanteren van gezonde stamcellen bijvoorbeeld een mogelijkheid.
Onderzoekers hebben muizen met zwaar beschadigde longen stamcellen laten inhaleren.
Na verloop van tijd herstelden bij die dieren alle longfuncties zich. Of denk aan het geven van een ‘revitalisatie-cocktail’ die stamcellen opkikkert.’
Stamcellen transplanteren
Zover is het nog niet. ‘We moeten nog veel uitzoeken en daarbij speelt de organoïde opnieuw een belangrijke rol.
Zo kunnen we daarop bijvoorbeeld testen of we bij het transplanteren van stamcellen een donor nodig hebben, of dat we de stamcellen van de patiënt zelf kunnen oplappen.
Ook kunnen we toetsen wat de beste techniek is om stamcellen op de juiste plek te krijgen, of wat de perfecte mix is om de stamcellen een boost te geven.
Het gebruik van mini-organen hierbij versnelt de zoektocht naar de medische oplossing natuurlijk enorm. Ons streven is om binnen vijf jaar met klinische studies in patiënten te kunnen starten.’
Exponentiële stijging
En hoe eerder we over een geneesmiddel beschikken hoe beter.
Nederland telt nu 600.000 mensen met de ongeneeslijke longziekte COPD en dat aantal neemt snel toe; men verwacht een groei naar meer dan 800.000 patiënten in 2040.
Jaarlijks overlijden er 7000 mensen aan COPD.
En de ziekte is in 2030 wereldwijd doodsoorzaak nummer drie, aldus de WHO. ‘Het moet sneller, met meer resultaten, en op kortere termijn,’ zegt directeur Michael Rutgers van het Longfonds. ‘Met LONGFONDS | Accelerate hebben we een cruciale stap gezet om een medische doorbraak in longonderzoek te versnellen.’
Michael Rutgers, directeur LongfondsBeeld Longfonds
Topwetenschappers
In het internationale programma LONGFONDS | Accelerate, werken gerenommeerde wetenschappers, academische pioniers, artsen, longpatiënten en maatschappelijke partners intensief samen.
Onder leiding van prof.dr. Hans Clevers (Hubrecht Instituut) en prof.dr. Carla Kim (Harvard Medical School/Boston Children’s Hospital) ontrafelen experts op het gebied van longziekten, celbiologie en longregeneratie hoe ze beschadigd longweefsel kunnen herstellen.
Een grote nalatenschap hebben we gebruikt als startkapitaal en we zetten ons in dit veelbelovende onderzoek te financieren tot echte oplossingen er zijn.
Rutgers: ‘In 2023 willen we concrete resultaten hebben.
Dan moet duidelijk zijn hoe longweefsel zich herstelt, is er een mini-long om onderzoek op te doen en er is een techniek om stamcellen te transplanteren.’
Bron: Volkskrant
![]()

Onder leiding van prof. dr. Hans Clevers van het Hubrecht Instituut werken topwetenschappers uit de Verenigde Staten en Europa de komende vijf jaar aan een minilong
Het Longfonds start een uniek internationaal onderzoeksprogramma BREATH om een oplossing voor longweefsel dat beschadigd is door COPD te versnellen.
Onder leiding van prof. dr. Hans Clevers van het Hubrecht Instituut werken topwetenschappers uit de Verenigde Staten en Europa de komende vijf jaar aan een minilong waarmee nieuwe medicijnen en behandelingen worden getest.
Een oplossing voor COPD is urgenter dan ooit.
Op dit moment lijden in Nederland bijna 600.000 mensen aan deze tot nu toe ongeneeslijke ziekte.
Naar verwachting stijgt dit aantal tot ruim 800.000 in 2040.
Mensen met COPD zijn vaak kortademig, moe en hoesten veel.
Dit komt door ontstekingen in hun longen en kapotte longblaasjes.
De wanden zijn zo beschadigd dat ze hun werk niet meer kunnen doen.
Stamcellen spelen in dit proces een sleutelrol.
Bij gezonde longen repareren stamcellen beschadigd weefsel, maar bij COPD is de schade zo langdurig en chronisch dat de stamcellen lijken uitgeput.
De schade aan de longen kan niet worden hersteld met de nu bestaande geneesmiddelen. BREATH richt zich op het ontwikkelen van behandelingen die dit proces juist omdraaien.
Eerste stap
De onderzoeksgroep van Clevers heeft al een belangrijke stap gezet.
Met stamcellen kunnen zij organoïden ontwikkelen, een soort mini-organen.
Nu is dat onlangs gelukt voor de luchtwegen.
De volgende stap is om dat ook te doen voor de longblaasjes.
Daarmee is heel gericht antwoord te vinden op de vraag waarom longblaasjes zich niet meer herstellen bij COPD.
Met deze minilongen kunnen medicijnen getest worden om de stamcellen in de longen te reactiveren.
Daarnaast onderzoekt het team of het herstelproces in de longen aangezet kan worden door gezonde stamcellen terug te plaatsen.
Medische doorbraak
Het doel is om over vijf jaar te starten met het testen van nieuwe behandelingen op patiënten met longstamcellen die beschadigd longweefsel kunnen herstellen.
Onderzoeksleider Hans Clevers: “Innovatieve ontwikkelingen binnen de regeneratieve geneeskunde brengen hoop op een oplossing voor de wereldwijd miljoenen longpatiënten met COPD. Als het lukt longweefsel te herstellen, realiseren we een medische doorbraak van wereldformaat.
Door de inspanningen van het Longfonds is het gelukt om internationaal onderzoekers, artsen, patiënten en maatschappelijk partners bij elkaar te brengen en deze doorbraak te versnellen.“
Impact COPD
De impact van de ziekte COPD op het dagelijks leven van patiënten is enorm.
Met de huidige medicijnen en behandelingen wordt geprobeerd de longen zo lang mogelijk goed te houden.
Toch raakt langzaam steeds meer longweefsel onherstelbaar beschadigd.
Michael Rutgers, directeur Longfonds: “Veel patiënten worden afhankelijk van zuurstof. Soms is een longtransplantatie hun enige hoop.
Meer dan 6.500 mensen sterven in Nederland jaarlijks aan de gevolgen van deze ziekte.
De grootste wens van mensen met COPD is het repareren van hun beschadigde longweefsel. Dat is nu nog niet mogelijk. Met het onderzoeksprogramma BREATH pakt het Longfonds de regie op om deze droom op korte termijn werkelijkheid te laten worden.”
Doodsoorzaak nummer 3
Alleen al in Nederland hebben ruim 600.000 mensen de ziekte COPD. COPD wordt veroorzaakt door ongezonde lucht die voortdurend in de longen komt bij het ademen, zoals door roken en luchtvervuiling.
Omdat de klachten bij COPD zich vaak pas na jaren openbaren, zal het aantal mensen met deze ziekte de komende jaren alleen maar toenemen. De voorspelling is dat COPD wereldwijd de derde doodsoorzaak is in 2030.
Longfonds | Accelerate
Op initiatief en onder regie van het Longfonds worden internationaal de krachten van vooraanstaande onderzoekers van academische instituten, artsen, longpatiënten en maatschappelijke partners gebundeld.
Door deze intensieve samenwerking en kennisdeling wordt een versnelde medische doorbraak mogelijk in de behandeling van de grote, nog ongeneeslijke longziekten zoals astma en COPD.
In januari 2018 startte het eerste onderzoeksprogramma naar het voorkomen van astma bij kinderen. Lees hier meer over Accelerate.
Bron: Zorg krant
![]()
0320